阿斯利康暂停新冠疫苗三期临床,康希诺、康泰生物表现各异
作者:马晓华
康希诺选择的也是腺病毒载体这条研发路径。
阿斯利康暂停腺病毒载体疫苗三期临床的消息,使得康希诺(688185.SH,06185.HK)、康泰生物(300601.SZ)8日的股市表现各异。
康希诺选择的也是腺病毒载体这条研发路径,目前三期临床研究尚无启动。康泰生物则是和阿斯利康的合作单位,拿到了阿斯利康的中国内地市场独家授权合作,通过技术转让推进阿斯利康与牛津大学合作的腺病毒载体新冠疫苗AZD1222在中国内地市场的研发、生产、供应和商业化。
8日上午,康希诺-U由跌转涨最高涨幅超8%,康希诺生物-B最高涨幅超7%,康泰生物则逼近20%跌停线。
康泰生物董秘苗向回应称,阿斯利康是全球新冠疫苗研发的公司中较为领先的,试验规模最大,出现个别案例是研发中的正常现象,不影响公司与阿斯利康合作的推进。
 8月14日,科学家在阿根廷布宜诺斯艾利斯省加林市的新冠疫苗研究实验室内工作,准备生产由英国牛津大学和英国制药公司阿斯利康合作开发的新冠疫苗。新华社图。
8月14日,科学家在阿根廷布宜诺斯艾利斯省加林市的新冠疫苗研究实验室内工作,准备生产由英国牛津大学和英国制药公司阿斯利康合作开发的新冠疫苗。新华社图。腺病毒载体疫苗也是中国的5条新冠疫苗研发技术路线之一,另外四条分别是灭活疫苗、重组蛋白疫苗、减毒流感病毒载体活疫苗和核酸疫苗。
9月2日,康希诺生物宣布已开始重组新型冠状病毒疫苗(Ad5-nCoV)的III期临床试验。已与俄罗斯制药公司NPO Petrovax Pharm,LLC(‘Petrovax’)签订协议,根据该协议,康希诺和Petrovax将共同推进在俄罗斯进行Ad5-nCoV的III期临床试验。公司和Petrovax已收到俄罗斯联邦卫生部关于Ad5-nCoV的临床试验申请批准,并在俄罗斯开始Ad5-nCoV的III期临床试验入组。此外,康希诺目前正在推动Ad5-nCoV的国际多中心III期临床试验,并计划在多个国家开展Ad5-nCoV的III期临床试验。
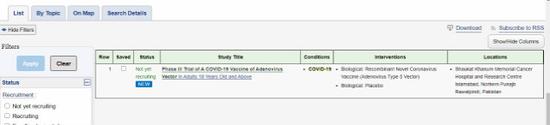
不过,第一财经记者查询政府注册机构(www.clinicaltrials.gov)发现,康希诺目前仅有位于巴基斯坦的三期临床项目进入登记系统,但还没有启动志愿者招募。
阿斯利康搁置新冠疫苗的三期临床试验,对腺病毒载体疫苗来说,也将是一个科学挑战。
目前,腺病毒载体技术平台尚未用于批准的疫苗中,但已在针对其他病毒(包括埃博拉病毒)的实验性疫苗中进行了测试。
今年5月,阿斯利康与牛津大学确立合作伙伴关系,在全球开发、生产和供应新冠疫苗AZD1222。阿斯利康发言人在声明中说,该公司的“标准审查程序触发了疫苗接种暂停,以允许审查安全数据。”发言人将暂停描述为“在一项试验中,只要其中一项试验可能存在无法解释的疾病,就必须采取常规行动,以确保试验的完整性。”该发言人还表示,该公司“正在努力加快对单个事件的审查,以最大程度减少对试验时间表的潜在影响。”
对于药物和疫苗的研发,临床搁浅并不少见。但是,由于迫切需要遏制新冠肺炎全球大流行的新方法,新冠疫苗的研发进展受到密切关注。9月4日,世卫组织举行新冠肺炎例行发布会,世卫组织首席科学家苏米娅·斯瓦米纳坦表示,全球已有超过30种新冠疫苗进入临床试验阶段,其中有9种新冠疫苗处于三期临床试验阶段。
阿斯利康的腺病毒载体新冠疫苗是第一个在三期临床试验被搁置的新冠疫苗。
版权及免责声明:凡本网所属版权作品,转载时须获得授权并注明来源“融道中国”,违者本网将保留追究其相关法律责任的权力。凡转载文章,不代表本网观点和立场。
延伸阅读
版权所有:融道中国