原标题:志愿者现不明疾病,英国“疫苗之光”被迫暂停实验!那美国的10亿美元订单怎么办?
资本市场对于新冠疫苗的火热期待,今天被泼了一盆冷水。
当地时间8日,英国制药公司阿斯利康宣布,由于一名参加该公司与牛津大学合作研发的新冠疫苗试验接种的志愿者出现疾病,该公司将暂停正在进行的一项疫苗试验。
这是首个宣布暂停的已进入三期临床试验的新冠候选疫苗。
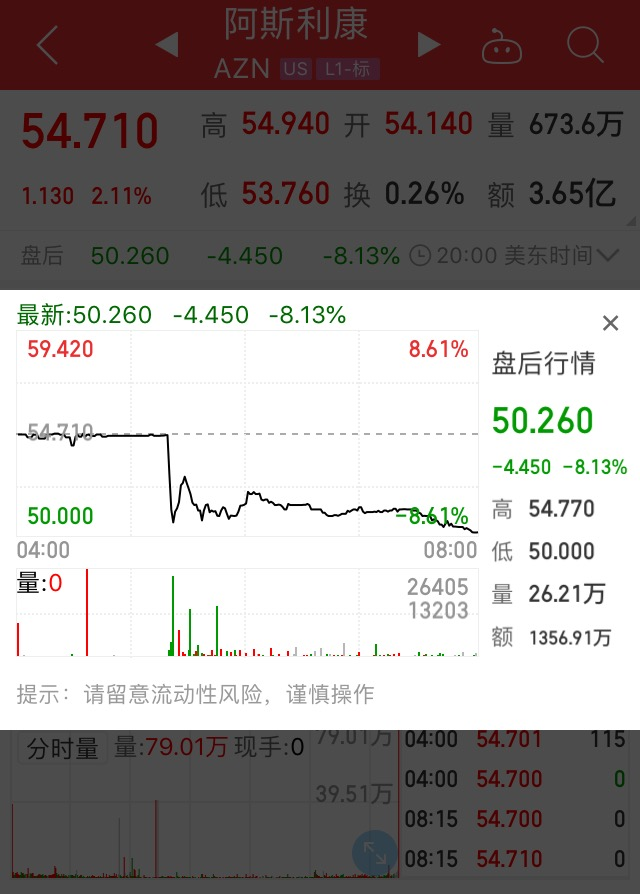
受此影响,阿斯利康在美国上市的股票周二盘后交易重挫逾8%。
由于中国疫苗企业康泰生物曾与阿斯利康签署协议,获得了其新冠疫苗在中国内地市场的独家授权。康泰生物9日开盘大跌,截至午间收盘,跌幅达19.61%,逼近跌停。此消息也带动A股疫苗概念大跌,多股跌幅接近10%。
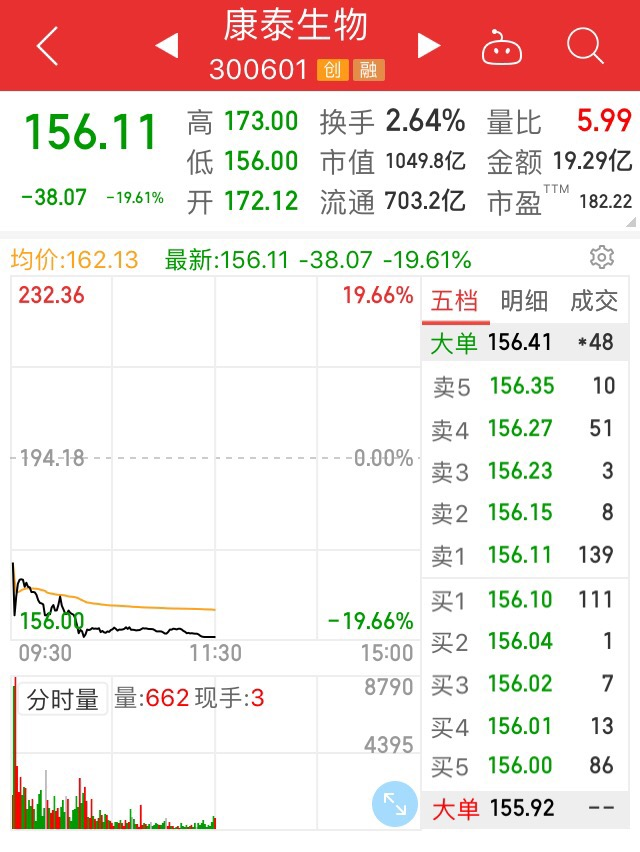
康泰生物对每日经济新闻回应称,出现个别案例是研发中的正常现象,不影响公司与阿斯利康合作的推进。
新冠疫苗志愿者现不明疾病
阿斯利康在一份声明中说,“我们已经启动标准审查程序并审查安全数据,暂停疫苗试验。这是一种常规行为,在调查过程中,一旦在某项试验中出现不明原因的潜在疾病,就必须采取这种行为,以确保试验的完整性。”
阿斯利康是英国最大制药公司。目前尚不清楚暂停试验是否由监管机构下令,也不清楚不良反应是什么。消息人士称,该志愿者“有望恢复”,但消息未得到证实。阿斯利康的新冠病毒疫苗是最早进入第三阶段临床试验的疫苗,根据《柳叶刀》7月发布的研究,该疫苗在第一阶段和第二阶段的试验中,60%的志愿者出现了副作用,包括发热、头痛、肌肉疼痛和注射部位有反应,这些副作用被描述为“轻度或中度”,并在试验过程中消退。
据美联社报道,健康新闻网站STAT称这一出现可能的副作用的志愿者来自英国,英国广播公司(BBC)的报道也给出了同样的说法。阿斯利康并未透露相关细节,只是将这种可能的副作用称为“一种潜在的原因不明的疾病”。CNN报道称,暂停试验的做法是疫苗试验中采取的正常预防性措施,以免给志愿者带来严重的影响。
一名该公司发言人证实,暂停的试验涉及美国等国。
更早前的8月31日,阿斯利康表示,该公司研制的新冠候选疫苗已在美国进入三期临床试验,这也是第三款在美国进行试验的新冠候选疫苗。
据美国有线电视新闻网(CNN)9月1日报道,该疫苗(AZD1222)由阿斯利康和英国牛津大学联合开发,并且得到了美国生物医学高级研究与发展管理局(BARDA)和美国国家卫生研究院(NIH)下属的过敏症与传染病研究所资助。

图片来源:阿斯利康官网
阿斯利康表示,目前正在招募近3万名18岁及以上的成年人进行试验,既包括健康人也包括有稳定的基础疾病的人,并且涵盖来自不同族裔和不同地方的志愿者。志愿者还包括艾滋病毒携带者以及新冠病毒感染风险更高的人群。
志愿者将分为疫苗组和对照组,均会进行两次注射,间隔四周。目前,阿斯利康疫苗的三期试验正在英国、巴西和南非进行,预计还将在日本和俄罗斯进行试验。阿斯利康表示,公司计划在全球范围内招募5万多名志愿者参与试验。
在阿斯利康疫苗之外,美国的莫德纳(Moderna)公司的疫苗、美国辉瑞(Pfizer)与德国生物新技术公司(BioNTech)合作研制的疫苗也已在美国政府的资助下在美国展开临床试验。
据英国金融时报之前报道,牛津大学和阿斯利康开发的新型冠状病毒疫苗在临床试验的第一阶段显示出令人鼓舞的结果。在《柳叶刀》发表的研究表明,这款疫苗产生了“强大的免疫反应”,而且所有受试者耐受。而早在今年5月,美国已同意支出10亿美元购买3亿剂阿斯利康开发的疫苗。
A股疫苗概念遭遇重挫
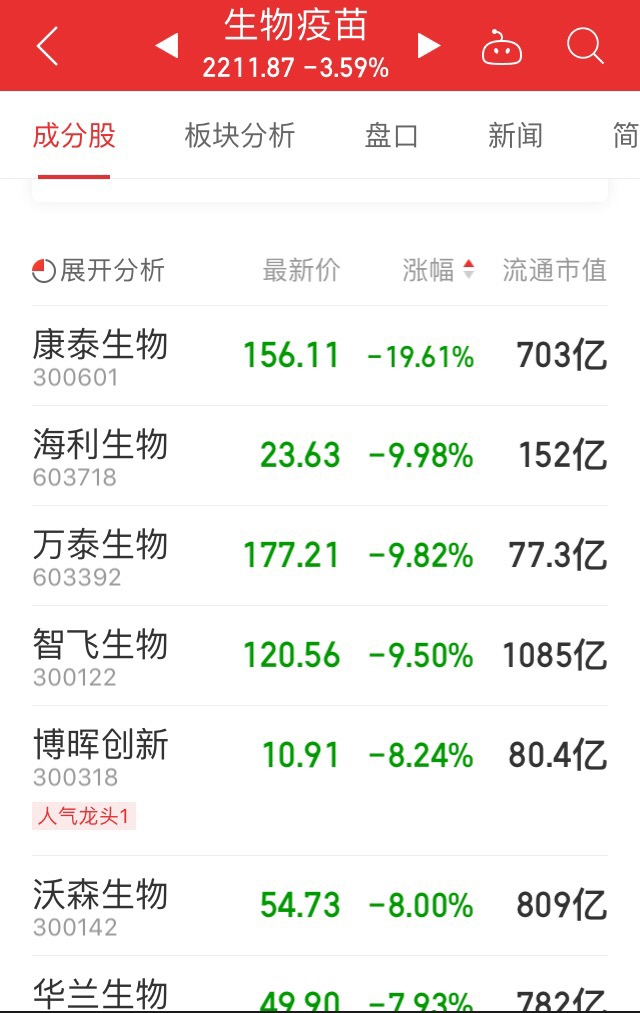
受阿斯利康叫停测试消息影响,A股生物疫苗概念9日遭遇重挫,截至午间收盘,康泰生物大跌19.61%,逼近跌停。智飞生物跌逾9.5%,万泰生物、海利生物逼近涨停,沃森生物、华兰生物等跌幅超7%。
今年8月初,阿斯利康曾宣布与康泰生物签署中国内地市场独家授权合作框架协议,通过技术转让积极推进阿斯利康与牛津大学合作的腺病毒载体新冠疫苗AZD1222在中国内地市场的研发、生产、供应和商业化。
每日经济新闻记者随即致电康泰生物,董秘苗向独家回应称,阿斯利康是全球新冠疫苗研发的公司中较为领先的,试验规模最大,出现个别案例是研发中的正常现象,不影响公司与阿斯利康合作的推进。对于这个事件,市场可能有所误解,阿斯利康已经经过了一二期的临床试验,如今出现的一个案例,只是研发过程中的小问题。
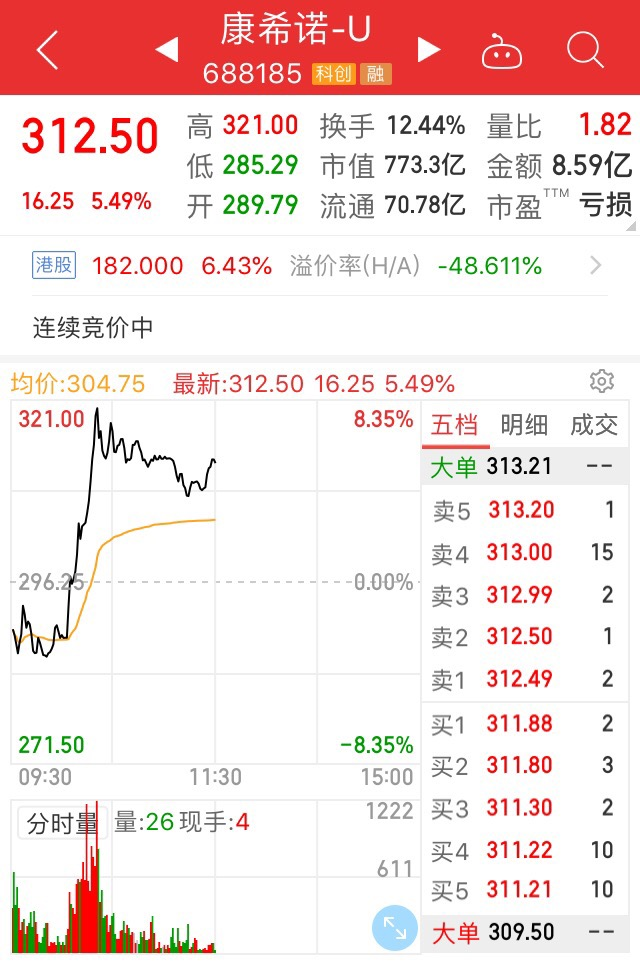
与此同时,与陈薇院士合作、最早参与新冠病毒疫苗之一的康希诺在今日疫苗股集体低走的势头下微微上扬。
截止午间收盘,康希诺由跌转涨5.49%,报价312.5元。
“从目前来看,我们的重组新冠疫苗对已经发生变异的新冠病毒能有效覆盖。”9月7日,“人民英雄”国家荣誉称号获得者、中国工程院院士、军事科学院军事医学研究院研究员陈薇接受新华社采访,就重组新冠疫苗安全性、有效性、临床试验进展情况一一进行了阐述,陈薇院士同时表示,年产3亿(剂)的目标是可以实现的,“我们正在努力扩大产能。”
这是短短一周时间里,军科院与康希诺生物重组新型冠状病毒疫苗(腺病毒载体)(Ad5-nCoV)再次传来的好消息。9月2日,康希诺生物公告称,该疫苗已开始与俄罗斯制药公司NPOPetrovaxPharm,LLC合作开展新冠疫苗第三阶段临床试验(大规模有效性临床研究),距离大规模使用又迈进了一大步。
美多数民众不愿第一时间接种新冠疫苗
突然出现的不明疾病不仅让制药公司遭遇挫折,更会让公众担忧疫苗安全。在美国,已有调查显示不少人出于安全原因不愿意接种疫苗。
据美国媒体报道,美国疾病控制和预防中心近日要求各州做好11月1日前“大规模”分发新冠疫苗的准备。
近日,《今日美国报》公布了和美国萨福克大学联合进行的一项民意调查结果。这项调查显示,出于对美国政府疫苗研发计划的不信任,有三分之二的美国民众表示他们不会在第一时间接种新冠疫苗。
这项对1000名美国人展开的民意调查显示,由于对美国联邦政府加速新冠疫苗研发感到担忧,只有27%的受访者表示会第一时间接种疫苗,而选择不会第一时间接种疫苗的受访者高达67%,其中44%的受访者表示,在别人接种疫苗之前,自己不会首先接种,23%的受访者表示,他们根本不会接种新冠疫苗。
《今日美国报》报道称,数十名医生、护士和卫生官员在接受采访时表示,他们对联邦政府这一决定感到担忧。美国流行病学专家也表示,美国公众对接种疫苗的抵制程度令人担忧,即便能生产3.3亿剂新冠疫苗,如果没人愿意接种,那也毫无意义。
一位来自马里兰州的受访者说,他不想接种疫苗是因为不想成为美国政府新冠疫苗试验的小白鼠。一名参与调查的医学人士更是直接表示,目前美国新冠疫苗还未完成临床试验,安全性存在风险。
全球九大药企CEO共签誓言:安全第一
9月8日,默沙东中国在其官方微信指出,九位生物制药企业CEO签署历史性誓言:在COVID-19疫苗研发中坚持以接种人的安全和健康为第一要务。

9月8日,阿斯利康、BioNTech、葛兰素史克、强生、默沙东(在美国和加拿大称作默克)、Moderna、诺瓦瓦克斯、辉瑞和赛诺菲九家生物制药企业CEO宣布一份历史性誓言,共同承诺在未来向全球监管机构提交COVID-19疫苗的申报资料和审批申请时将坚守科学诚信。
九位CEO签署了以下誓言承诺:
在潜在的COVID-19疫苗研发及试验中将严格遵守高标准的伦理要求和坚实可靠的科学原则。疫苗的安全性和有效性,包括任何潜在COVID-19疫苗在内,都会经过全球专业监管机构的评估和确认,如美国食品药品监督管理局(FDA)。FDA已为COVID-19疫苗的研发做出了明确的指导准则,并为疫苗在美国的潜在授权和获批设立了明确标准。FDA的指导和标准基于必要的科学原则与医学原则,试验要在这些原则之上明确体现潜在COVID-19疫苗的安全性和有效性。具体而言,FDA要求用于申请监管审批的科学证据必须来自大量、高质量的随机、盲测者参与的临床试验,需要有恰当的研究设计、来自多元人群的大量参与者。
在遵循FDA等专业监管机构就COVID-19疫苗研发所给出的指导意见、与现有标准和实践保持一致、以公共卫生利益为先的前提下,九家企业CEO宣誓:永远以接种人的安全与健康为第一要务
在开展临床试验和严谨的生产过程中,始终秉持科学和伦理的高标准。
三期临床试验的设计和开展将依据FDA等专业监管机构的要求进行,只有在三期临床试验结果显示足够的安全性和有效性后,才会申请批准或紧急使用授权。
努力保证疫苗有充分的供应和充足的选择,包括适合全球广泛使用的疫苗。
(本文内容仅供参考,不作为投资依据。投资者据此操作,风险自担。)
版权及免责声明:凡本网所属版权作品,转载时须获得授权并注明来源“融道中国”,违者本网将保留追究其相关法律责任的权力。凡转载文章,不代表本网观点和立场。
延伸阅读
版权所有:融道中国